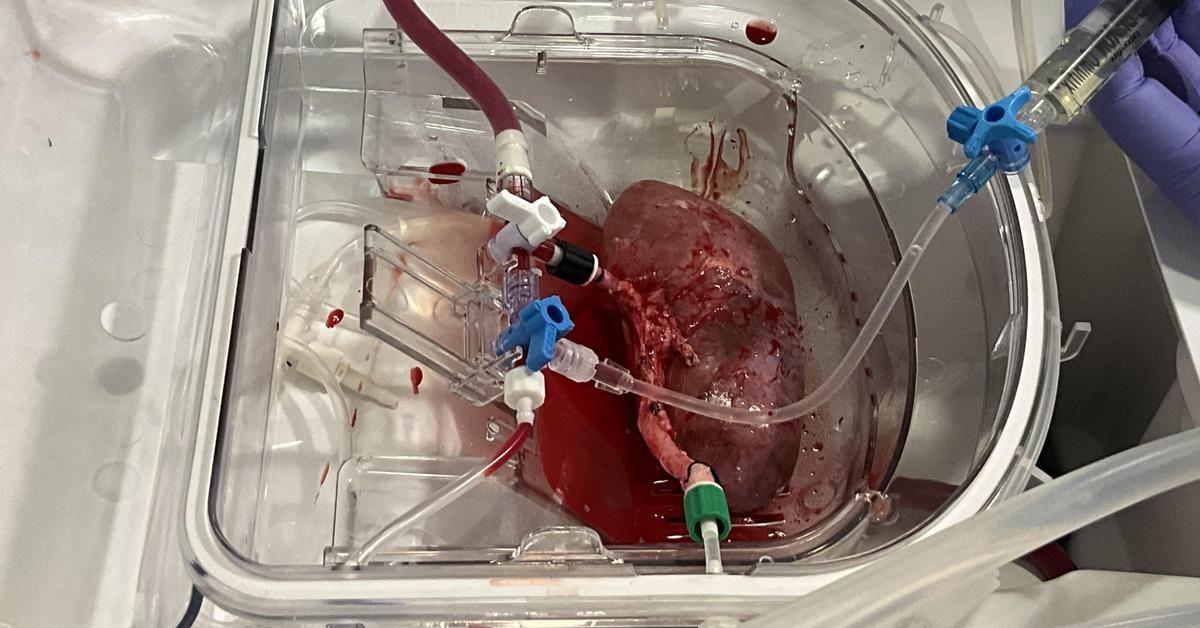
Un equipo internacional de investigadores, liderados por científicos españoles, ha logrado por primera vez producir organoides renales humanos, combinarlos con riñones de cerdo fuera del cuerpo del animal y trasplantarlos de nuevo al animal de una manera viable, sin que se registraran daños o toxicidad.
Los organoides son estructuras tridimensionales, similares a un órgano diminuto, creadas en el laboratorio a partir de células tumorales o madre —que dan origen a otros tipos de células— de una persona. Aunque no se trata de un órgano completo, sí logran reproducir muchas de sus estructuras y sus funciones principales.
Permiten, por tanto, estudiar cómo se desarrolla el riñón, probar nuevos fármacos y, en el futuro, podrían ser utilizados para reparar tejidos renales dañados o mejorar órganos destinados al trasplante.
El trasplante ha sido posible gracias a la implicación de numerosos centros de investigación de varios países, liderados por el Instituto de Bioingeniería de Catalunya (IBEC), en colaboración con el Instituto de Investigación Biomédica de A Coruña (INIBIC), la Organización Nacional de Trasplantes (ONT) o el Instituto de Salud Carlos III. Los resultados del trabajo se han publicado este viernes en la revista Nature Biomedical Engineering .
El estudio describe por primera vez un método sistemático y escalable para producir miles de estos organoides renales humanos, utilizando técnicas de 'microagregación' e ingeniería genética
El estudio, que fue liderado por la investigadora Núria Montserrat —en la actualidad, consejera de Investigación y Universidades de la Generalitat de Catalunya—, representa un hito en el campo de la medicina regenerativa y personalizada, ya que establece las bases para la utilización de los organoides de riñón derivados de células madre humanas para terapia celular en ensayos clínicos.
Es la primera vez que se consigue combinar organoides renales humanos con riñones porcinos vivos, conectados a máquinas de 'perfusión normotérmica'. Estas máquinas son los dispositivos que se usan habitualmente en el quirófano para mantener el órgano vivo y oxigenado fuera del cuerpo antes de un trasplante. Los investigadores han logrado insertar esos organoides humanos dentro de los riñones porcinos y monitorear en tiempo real su integración y su función.
Objetivo: aumentar el número de órganos viables para el trasplante
“Nuestra investigación demuestra que la combinación de tecnologías de organoides y perfusión ex vivo puede permitir intervenciones celulares en condiciones totalmente controladas”, ha explicado Núria Montserrat en una nota difundida por el IBEC, donde añade que el objetivo a largo plazo es poder regenerar o reparar un órgano antes del trasplante. Esto podría reducir el tiempo de espera de los pacientes crónicos y aumentar el número de órganos viables para el trasplante.
El estudio describe por primera vez un método sistemático y escalable para producir miles de estos organoides renales humanos, utilizando técnicas de 'microagregación' e ingeniería genética.
Nuestro nuevo método abre la puerta a aplicaciones como la detección de fármacos o el estudio de enfermedades
Elena Garreta — Investigadora
El equipo de investigación observó que, después de 24 y 48 horas del trasplante, los organoides humanos persistían integrados en el tejido renal porcino, mantenían su viabilidad y no desencadenaban ninguna respuesta inmune significativa, y que el riñón trasplantado continuaba funcionando con normalidad sin que se detectaran signos de daño ni toxicidad.
Los investigadores han apuntado que esta metodología permite augurar un escenario clínico en el que los órganos destinados al trasplante puedan ser tratados y acondicionados antes de implantarlos.
Detectar fármacos y estudiar enfermedades
La investigadora Elena Garreta, del grupo de 'Pluripotencia para la regeneración de órganos' del IBEC y coautora del estudio, ha subrayado que a pesar del gran potencial clínico de los organoides, uno de los grandes retos para aplicar esta tecnología en tratamientos médicos reales era conseguir producirlos de manera escalable, uniforme y asequible.
“Ahora, con nuestro nuevo método, podemos generar miles de organoides renales en condiciones controladas y en poco tiempo, con una gran precisión y sin necesidad de componentes complejos, lo que abre la puerta a aplicaciones como la detección de fármacos o el estudio de enfermedades”, ha asegurado la investigadora.
La directora de la Organización Nacional de Trasplantes, Beatriz Domínguez-Gil González, ha subrayado que el trabajo se encuentra todavía en una fase pre-clínica, pero representa un paso muy relevante en el desarrollo de nuevas estrategias de medicina regenerativa. Asimismo, ha señalado que aunque cualquier aplicación en humanos está aún lejos en el tiempo “podemos vislumbrar un futuro en el que los organoides humanos permitan reparar o regenerar órganos dañados”.
Eso podría, a largo plazo, reducir la necesidad de trasplantes y aumentar la disponibilidad de órganos viables para uso clínico, ha manifestado a EFE la directora de la ONT, co-autora también del estudio. Domínguez-Gil asegurado que si la tecnología probada demuestra su eficacia y seguridad en todas las fases “podría abrir la puerta a regenerar órganos antes de proceder a su trasplante”, lo que permitiría recuperar órganos que hoy no son aptos para uso clínico y acortar los tiempos de espera.
Según datos del Observatorio Global de Donación y Trasplante —gestionado por la Organización Nacional de Trasplantes (ONT) como centro colaborador de la OMS—, en 2024 se realizaron 173.448 trasplantes de órganos en el mundo (datos procedentes de 92 países). La OMS estima, no obstante, que esa cifra apenas cubre un 10 por ciento de las necesidades globales de trasplante, que continúan creciendo por el aumento de enfermedades crónicas no transmisibles.

 ElDiario.es
ElDiario.es
 Noticias de España
Noticias de España CNN
CNN FOX News Videos
FOX News Videos Raw Story
Raw Story